- TOP
- 製品情報
- Loopamp製品(臨床検査分野) 一覧
- Loopamp H1 pdm 2009インフルエンザウイルス検出試薬キット
インフルエンザウイルス核酸キット Loopamp H1 pdm 2009インフルエンザウイルス検出試薬キット
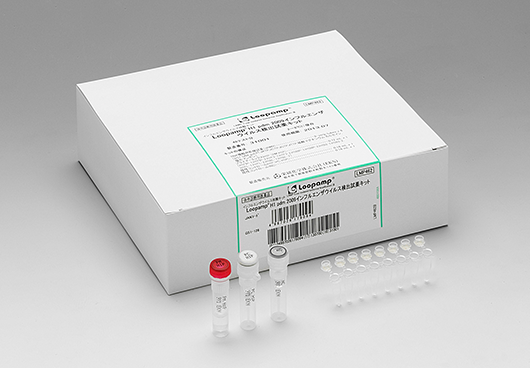
製品概要
- RT-LAMP法によりヒト由来検体中のインフルエンザA(H1N1)pdm RNAを特異的に検出します。
- RT-LAMP法とはLAMP法を応用し逆転写酵素を用いてRNAをターゲットとして増幅を行う核酸増幅法です。
- 反応チューブのフタに乾燥化した試薬が固相してあるため試薬調製等が不要で操作が簡単です。
- LAMP反応に要する時間は約35分です。
- 核酸抽出は、Loopamp ウイルスRNA抽出試薬(別売)を使用して簡易に行うことができます。
使用目的
鼻腔拭い液又は咽頭拭い液から抽出されたインフルエンザA(H1N1)pdm RNAの検出(インフルエンザA(H1N1)pdm感染が疑われる有症状者を対象とする診断の補助)
製品仕様
| 製品名 | Loopamp H1 pdm 2009インフルエンザウイルス検出試薬キット |
| 測定方法 | LAMP法(定性検出キット) |
| 対象検体 | 鼻腔拭い液又は咽頭拭い液 |
| 最小検出感度 | 80コピー/テスト |
| 製品コード | LMP462 |
| 包装単位 | 48テスト分 |
| 貯蔵方法 | 2~8℃ |
| 有効期間 | 6ヵ月間 |
| キットの構成 | RNA増幅用乾燥試薬(dRMR)・・・ 8-strip tubes ×6 プライマーミックスH1P(PM H1P)・・・ 0.72 mL×1 陽性コントロールH1P(PC H1P)・・・ 0.16 mL×1 陰性コントロール(NC)・・・ 0.16 mL×1 |
- Loopampは栄研化学株式会社の登録商標です。
使用上又は取扱い上の注意については添付文書をご参照ください。(情報提供年月:2021年7月)
重要な基本的注意
- 本製品の検査対象はインフルエンザA(H1N1)pdm(以下 AH1pdm)感染が疑われる有症状者とすること。
- 本製品で判定が陰性であっても、疾患としてのAH1pdm感染を否定するものではない。
- 診断は、本製品による検査結果のみで行わず、厚生労働省の最新の症例定義を参照し、臨床症状も含めて総合的に判断すること。本製品はあくまでもAH1pdm感染が疑われる有症状者を対象とする診断の補助を行うためのものである。
- 本製品の臨床性能試験におけるPandemic(H1N1)2009患者検体の陽性率は次のとおりであった。
厚生労働省健康局結核感染症課長通知(健感発0722第2号)の症例定義により新型インフルエンザ(Pandemic(H1N1)2009)確定例とみなされた症例から得られた検体について、本製品による陽性率は検体種別に鼻腔拭い液(簡易抽出サンプル溶液):96.6%(85/88)、咽頭拭い液(簡易抽出サンプル溶液):100.0%(41/41)、鼻腔拭い液(精製サンプル溶液):96.6%(85/88)、咽頭拭い液(精製サンプル溶液):92.7%(38/41)であった。
一方、非新型インフルエンザ(非Pandemic(H1N1)2009)患者の検体に対する本製品による陰性率は検体種別に鼻腔拭い液(簡易抽出サンプル溶液):89.3%(25/28)、咽頭拭い液(簡易抽出サンプル溶液):93.8%(15/16)、鼻腔拭い液(精製サンプル溶液):85.7%(24/28)、咽頭拭い液(精製サンプル溶液):100.0%(16/16)であった。
尚、リアルタイム濁度検出による判定結果と蛍光目視検出による判定結果とは全例一致した。
関連製品
お問い合わせ
本製品の製造販売元は栄研化学株式会社です。
製品および購入に関するお問い合わせは お問い合わせフォーム よりお願いいたします。
ピックアップ製品
NEW Loopamp マラリアPan検出試薬キット、他2品目
Loopamp 新型コロナウイルス2019(SARS-CoV-2)検出試薬キット
Loopamp Aspergillus fumigatus 検出試薬キット